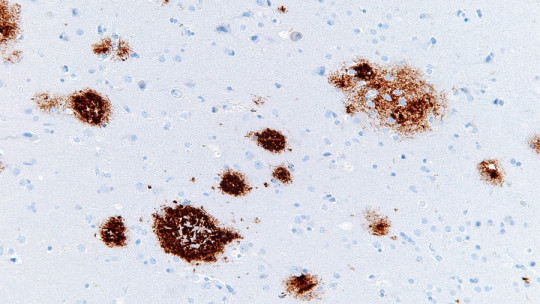
Las placas seniles se producen en la sustancia gris del cerebro por la acumulación de la proteína beta-amiloide, que según los investigadores figura como una de las proteínas candidatas a la hora de explicar el origen y el mantenimiento de enfermedades como el Alzheimer.
En este artículo veremos qué son y cómo se originan las placas seniles, cuál es su relación con la enfermedad de Alzheimer y qué tratamientos se han puesto en marcha para combatir su presencia.
- Artículo relacionado: "Tipos de demencias: las 8 formas de pérdida de cognición"
¿Qué son las placas seniles?
Las placas seniles, también conocidas como placas neuríticas o placas amiloides, se forman en la sustancia gris del cerebro a partir de la acumulación de depósitos extracelulares de neuritas distróficas y degeneradas, microglía y astrocitos reactivos, y de una proteína llamada beta-amiloide.
Esta proteína se produce mediante un corte en la secuencia de aminoácidos de la proteína precursora del amiloide (PPA) y cumple funciones específicas en procesos de estrés oxidativo, el transporte de colesterol o la actividad antimicrobiana, entre otras.
Por su parte, la PPA es una proteína que se sintetiza en los espacios interneuronales, en las células del músculo liso de la pared vascular y en las plaquetas. Se ha sugerido que esta proteína actúa como un receptor que se acopla a otras proteínas transductoras de señales químicas, siendo la responsable, junto con células agregadas y otras fibras nerviosas alteradas, de que se formen las placas seniles.
Una vez formadas, las placas seniles se distribuyen por multitud de regiones del encéfalo, como la corteza cerebral, los ganglios basales, el tálamo o el cerebelo. Se pueden distinguir hasta tres tipos de placas seniles: las placas difusas, las placas amiloideas y las placas compactas o neuríticas.
Las placas difusas están constituidas por depósitos de amiloide no fibrilar que no alteran el neuropilo (un conjunto de prolongaciones neuronales, axones y dendritas, y prolongaciones gliales que las envuelven), ni provocan una respuesta de la glía, por lo que su presencia no suele acarrear un deterioro cognitivo en la persona portadora.
Las placas amiloideas contienen un centro más o menos denso; y las las placas compactas o neuríticas son las que tienen una naturaleza tóxica y son específicas de enfermedades neurodegenerativas como el Alzheimer, debido a que contienen placas seniles, astrocitos y microglía activada).
Placas amiloides y enfermedad de Alzheimer
La enfermedad de Alzheimer se caracteriza por la acumulación de ovillos neurofibrilares (conglomerados anormales de proteínas) y depósitos de proteína beta-amiloide, la responsable de que se formen las placas seniles, como hemos comentado al principio.
Estas anormalidades provocan la muerte neuronal en estructuras cerebrales muy importantes, como el hipocampo y la corteza, implicadas en procesos de aprendizaje y memoria. Esta muerte neuronal es precedida por una pérdida progresiva de sinapsis y una alteración en la plasticidad neuronal del paciente, que precipita la aparición de los síntomas cognitivos típicos de esta enfermedad.
Se postula que es el desequilibrio entre la formación y la eliminación de beta-amiloide, y su posterior acumulación, el que desencadena los eventos negativos (como la disfunción sináptica, la inflamación glial o la hiperfosforilación) que desembocan en dicha muerte neuronal.
Las placas seniles también pueden estar presentes en el cerebro de personas sanas que no presentan ningún síntoma, especialmente a edades avanzadas. Y todavía se desconoce el motivo por el cual algunas personas son más resistentes que otras a la acumulación de estas placas. Lo que sí se ha demostrado fehacientemente es que en todas las personas que sufren la enfermedad de Alzheimer se encuentra presencia de placas amiloides.
- Quizás te interese: "Alzheimer: causas, síntomas, tratamiento y prevención"
La “cascada amiloide”
La hipótesis de la “casaca amiloide” es uno de los modelos más destacados e influyentes empleados para explicar el origen y la evolución de la demencia más común del mundo, como es la enfermedad de Alzheimer.
Esta hipótesis se sustenta sobre la idea de que es una cascada química la que termina provocando la acumulación de las placas seniles en el cerebro y la posterior destrucción neuronal y pérdida de facultades cognitivas. Dicha acumulación marcaría el inicio patológico de la demencia en cuestión.
Los daños provocados se deberían, según esta hipótesis, a una excesiva formación de proteína beta-amiloide o, en todo caso, a un déficit en su eliminación, un proceso que provoca la degeneración y atrofia de algunas estructuras cerebrales del paciente.
Con todo, las respuestas a la pregunta de qué es lo que desencadena esta cascada química siguen siendo controvertidas. La mayoría de las investigaciones que se han realizado al respecto han tratado de buscar fármacos capaces de frenar o reducir el avance de la demencia basándose en la idea de que el objetivo es interrumpir la acumulación de estas proteínas dañinas.
Sin embargo, a día de hoy sigue sin haber un consenso al respecto de cuáles son los factores desencadenantes. Se sugiere que podrían serlo fallos genéticos raros que provocarían anomalías en el ADN que codifica la proteína precursora de amiloide, que es la responsable de sintetizar la beta-amiloide. Y este error genético conduciría a la formación de los depósitos anormales que generarían las placas seniles.
Otra teoría apuntaría a que el problema no sería de la proteína precursora, sino más bien de otra proteína que se encarga de eliminarla. En cualquier caso, ambas teorías sugieren que el marcador principal del inicio patológico de la demencia y la enfermedad de Alzheimer tendría que ver con la cascada amiloide.
Anticuerpos para combatir a las placas seniles
En los últimos años se viene investigando el uso de la inmunoterapia, un tratamiento dirigido a estimular las defensas naturales del cuerpo, para ayudar en el tratamiento de enfermos de Alzheimer. Se estudia de qué forma los anticuerpos podrían penetrar en las neuronas y reducir las proteínas beta-amiloides que forman las placas seniles.
Los investigadores han utilizado ratones para exponerles a inmunoanticuerpos, de modo que se puedan examinar los cambios producidos en las células mediante el uso del microscopio, la inmunofluorescencia y otras técnicas más avanzadas. Su descubrimiento radica en que los anticuerpos se unen a la proteína beta-amiloide, en una zona específica del precursor de la proteína, que se encuentra en el exterior de la célula.
Este complejo de anticuerpos penetraría en la célula, reduciendo los niveles de beta-amiloide y construyendo bloques de placas que se encuentran fuera y entre las células. El anticuerpo reduciría a prácticamente un tercio la acumulación intracelular de la proteína.
Además, se han hallado evidencias de que los anticuerpos podrían inhibir la actividad de dos enzimas (las beta-secretasas) que facilitan la producción de proteína amiloide. Se cree que los anticuerpos podrían incrementar la degradación de beta-amiloide más que inhibir su producción, aunque todavía no está claro.
El hallazgo científico de que los anticuerpos podrían actuar tanto dentro como fuera de las células conlleva implicaciones significativas de cara a poder investigar otras enfermedades neurodegenerativas y trastornos autoinmunes.
Referencias bibliográficas:
- Gra, M.S., PN Padrón, RJJ Llibre. (2002). Péptido β amiloide, proteína Tau y enfermedad de Alzheimer. Rev Cubana Invest Biomed 21, 253-261.
- Hardy, J., Selkoe DJ. (2002) The amyloid hypothesis of Alzheimer’s www.neurologia.com Rev Neurol 2010; 51 (8): 471-480 479 Diagnóstico precoz de la enfermedad de Alzheimer: fase prodrómica y preclínica disease: progress and problems on the road to therapeutics. Science; 297: 353-6.
- Simón, A.M., Frechilla D., Del Río J. (2010). Perspectivas sobre la hipótesis de la cascada del amiloide en la enfermedad de Alzheimer. Rev Neurol; 50: 667-75