El tiempo pasa para todos, y eso es una realidad innegable. Concebir la vida sin la muerte es imposible, pues toda materia orgánica se degrada, pierde forma y se transforma. Sin ir más lejos, la definición más adecuada que se nos ocurre para definir la vida desde un punto de vista biológico es la siguiente:el estado intermedio entre el nacimiento y la muerte.
El tiempo pasa de forma inalienable, sí, pero te sorprenderá saber que no lo hace igual para todos. La edad cronológica (cronométrica) indica el movimiento de las manecillas del reloj, pero esta magnitud física no tiene nada que ver con lo que sucede en el interior de nuestros cuerpos. Las fases de un proceso biológico no poseen la misma cualidad o índole que las de un proceso físico en tanto que meramente sucesivo.
En el estudio fisiológico de los seres vivos, las fases de un proceso vienen determinadas por las dinámicas “del proceso intrínseco”, y no por las imposiciones de un elemento físico, como puede ser un reloj. Así, una persona alcohólica de 40 años puede tener el hígado de una de 80, por ejemplo, mientras que un atleta octogenario puede presentar la musculatura del tren inferior típica de una persona sedentaria de 60 años. El tiempo pasa, sí, pero la edad biológica puede ser diferente a lo que indica el calendario.
Muchos de los parámetros que modifican la edad biológica de los tejidos vivos están completamente ligados al estilo de vida del individuo, pero existen otros conceptos complejos y fascinantes que explican, en parte, por qué el proceso de envejecimiento celular es único e intercambiable. Te explicamos el secreto de la vida y la muerte con un término tan apasionante como útil: conócelo todo sobre los telómeros.
- Artículo relacionado: "¿Cuáles son las diferencias entre la edad cronológica y la edad biológica?"
¿Cómo se organizan los cromosomas y dónde están los telómeros?
Empecemos desde el principio, como la vida misma. Los seres humanos presentamos, en cada una de nuestras células, el ADN encerrado en un núcleo. Mediante una serie de procesos que aquí no nos competen, la información del ADN es transportada del núcleo a los ribosomas del citoplasma celular, para que estos puedan sintetizar proteínas. La síntesis proteica es la base del metabolismo de los seres vivos, así que se podría decir que el ADN contiene toda la información necesaria para que la vida sea tal.
En los seres humanos, el ADN se condensa en cromatina, formando cromosomas. Cada célula no sexual de nuestro cuerpo (de forma general) posee 23 pares de cromosomas (46 totales), de los cuales 23 provienen del gameto femenino (n) y 23 del masculino (n), que al juntarse forman un cigoto (2n). Las partes de un cromosoma son las siguientes:
- Película y matriz: cada cromosoma está delimitado por una membrana que encierra una sustancia gelatinosa.
- Cromonemas: estructura filamentosa que compone cada una de las cromátidas hermanas (siendo una cromátida cada mitad del cromosoma con forma de “X”)
- Cromómeros: sucesión de gránulos que acompañan al cromonema en su longitud.
- Centrómero: lugar donde las dos cromátidas hermanas se juntan. Para que nos entendamos, es el centro de la “X”.
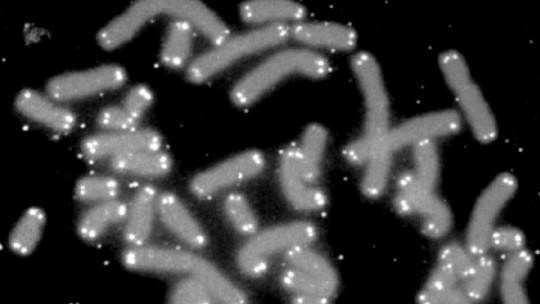
- Telómeros: las partes terminales del cromosoma, sus “puntas”.
Nos hemos dejado alguna sección específica en el tintero con la finalidad de no perdernos en tecnicismos, pero ya nos hemos encontrado por primera vez con el término que aquí nos atañe. Es hora de explorarlo a fondo.
¿Qué son los telómeros?
En base a lo que hemos visto hasta ahora, el telómero se define casi por sí solo: es la punta del cromosoma. Los telómeros son regiones de ADN no codificante (no tienen información necesaria para la síntesis de proteínas) altamente repetitivas, cuya función es otorgar estabilidad a los cromosomas en las células eucariotas a lo largo de su vida. En base a la existencia de estas estructuras, podemos explicar de forma parcial dos fenómenos que quitan el aliento a todo ser humano: el envejecimiento y el cáncer. Veamos cómo.
1. Durante la duplicación del ADN, los telómeros no se replican enteros
Las células somáticas se dividen por mitosis y, para que esto sea posible, se tiene que duplicar el ADN de la célula primigenia que dará lugar a la estirpe de descendientes. Con cada proceso de replicación, y debido a ciertas características de las enzimas que lo hacen posible, los telómeros se van acortando.
La longitud de los telómeros en humanos decrece a una tasa de 24,8-27,7 pares de bases por año. Con el tiempo y la división celular, los telómeros de los cromosomas de las células descendientes se vuelven tan cortos que la célula ya no puede dividirse y, por tanto, con la muerte de las últimas entidades celulares se produce la muerte del tejido. Haciendo un paralelismo de “andar por casa”, es como si quitamos un poco de agua cada vez que la pasamos de un vaso a otro. Al principio puede no notarse, pero después de repetir X veces el proceso, ya no se puede hacer el trasvase, pues no queda agua que trasladar.
Por esta razón, se dice que los telómeros son un excelente marcador de la edad biológica: en base a su longitud, los científicos pueden estimar cuánto le queda por delante a un grupo celular y, por tanto, al organismo entero. El acortamiento telomérico es parte del proceso de envejecimiento normal, pero ciertos agentes asociados a un estilo de vida específico pueden fomentar el daño del ADN cromosómico y, por ende, a un acortamiento más rápido de los telómeros.
- Quizás te interese: "Cromosomas: qué son, características y funcionamiento"
2. La importancia de la telomerasa
Hemos explicado el mecanismo de la vejez, pero la cosa se pone aún más interesante si conocemos que, por increíble que parezca, el propio cuerpo tiene la solución para la inmortalidad a nivel teórico, al menos en los primeros estadios de vida.
La telomerasa es una enzima encargada de mantener la longitud de los telómeros mediante la adición de secuencias genéticas repetidas. Este proceso biológico tiene “truco”: la actividad está presente en las células de la línea germinal y ciertas células hematopoyéticas, pero las células somáticas maduras inhiben su funcionalidad después del nacimiento. Así, es el propio organismo el que codifica su degradación programada.
3. Los telómeros y el cáncer
Estudios actuales sugieren que los seres humanos podríamos revertir el proceso de senescencia celular si incrementásemos artificialmente la actividad telomerasa en las células somáticas que forman los tejidos de nuestro cuerpo. Por desgracia, esto podría llegar a tener un doble efecto: en ambientes experimentales, si se estimula la actividad telomerasa y se inactivan ciertos genes de supresión tumoral, tiene lugar una inmortalización celular que promueve significativamente la aparición de un tumor.
Vamos más allá en esta línea de pensamiento, pues el 75-80% de los cánceres surgido a partir de células somáticas presentan actividad telomerasa. Esto no quiere decir necesariamente que la telomerasa cause cáncer, pero todo parece indicar que los niveles altos de esta enzima son un claro indicativo de la posible malignidad de un tumor. Si una célula es inmortal, esta puede replicarse indefinidamente: estamos explicando casi palabra por palabra la formación de un cáncer.
En base a esta premisa, se están desarrollando en el ámbito experimental diversos tratamientos anti-telomerasa. En cultivos celulares, los resultados son cuanto menos prometedores: en algunas líneas celulares cancerígenas, al inhibir la actividad de la telomerasa, se produce una muerte espontánea de la estirpe tras unas 25 divisiones, pues los telómeros se acortan y no pueden ser repuestos de ninguna manera.
Resumen
Tras la exposición de datos como estos, es imposible no sentirse esperanzados. El cáncer es uno de los problemas de salud más importantes y trágicos a día de hoy, pues tras cada muerte y cada cifra hay una historia de lucha, tristeza y esperanza. Un tumor neoplásico no es solo una agrupación de células que crecen de forma descontrolada: es miedo, una batalla de la ciencia contra la fisiología, aceptación o negación y, en el peor de los casos, la pérdida temprana de una vida.
Los mecanismos de senescencia celular nos ayudan a entender el envejecimiento de los tejidos y el proceso que nos lleva hacia la muerte, pero el objetivo final no es encontrar la inmortalidad. El verdadero reto, a día de hoy, es salvar todas aquellas vidas que penden de un hilo por un grupo de células rebeldes que mutaron para volverse en contra de su hospedador.
Referencias bibliográficas:
- Arvelo, F., & Morales, A. (2004). Telómero, telomerasa y cáncer. Acta Científica Venezolana, 55, 288-303.
- Couto, A. B. (2008). Telomerasa: fuente de juventud para la célula. Medisur: Revista Electrónica de las Ciencias Médicas en Cienfuegos, 6(2), 68-71.
- La influencia en el estilo de vida de los telómeros y longevidad, genotipia. Recogido a 4 de marzo en https://genotipia.com/estilo-vida-telomeros-longevidad/
- Membrive Moyano, J. (2017). La enzima telomerasa como diana terapéutica.
- Moyzis, R. K. (1991). El telómero humano. Investigación y ciencia, (181), 24-32.
- Salamanca-Gómez, F. (1997). La telomerasa. Inmortalizar sin malignizar. Gac Med Mex, 8, 385.
- Telómero, NIH. Recogido a 4 de marzo en https://www.genome.gov/es/genetics-glossary/Telomero
- Vargas, E., & Espinoza, R. (2013). Tiempo y edad biológica. Arbor, 189(760), 022.